البيئة المحيطة قد تسرّع الشيخوخة الدماغية أكثر من نمط الحياة
![]() روسيا والصين يبحثان خفض التصعيد في الشرق الأوسط
روسيا والصين يبحثان خفض التصعيد في الشرق الأوسط
![]() ارتفاع أسعار النفط
ارتفاع أسعار النفط
![]() الكويت: الدفاعات الجوية تتصدى لهجمات صاروخية وطائرات مسيرة معادية
الكويت: الدفاعات الجوية تتصدى لهجمات صاروخية وطائرات مسيرة معادية
![]() هبوط أسعار الذهب بالمعاملات الفورية
هبوط أسعار الذهب بالمعاملات الفورية
![]() طقس الاثنين.. أمطار رعدية غزيرة وسيول وبرد على عدة مناطق
طقس الاثنين.. أمطار رعدية غزيرة وسيول وبرد على عدة مناطق
![]() وزارة الدفاع: اعتراض وتدمير مسيّرتين خلال الساعات الماضية
وزارة الدفاع: اعتراض وتدمير مسيّرتين خلال الساعات الماضية
![]() التعشير يحيي مزارع الورد الطائفي ويعكس إرثًا زراعيًّا وثقافيًّا متجددًا
التعشير يحيي مزارع الورد الطائفي ويعكس إرثًا زراعيًّا وثقافيًّا متجددًا
![]() مستشفى الملك فهد بالباحة يُدخل تقنية متقدمة لعلاج أمراض المفاصل
مستشفى الملك فهد بالباحة يُدخل تقنية متقدمة لعلاج أمراض المفاصل
![]() تنسيق روسي صيني لخفض التصعيد في الشرق الأوسط
تنسيق روسي صيني لخفض التصعيد في الشرق الأوسط
![]()
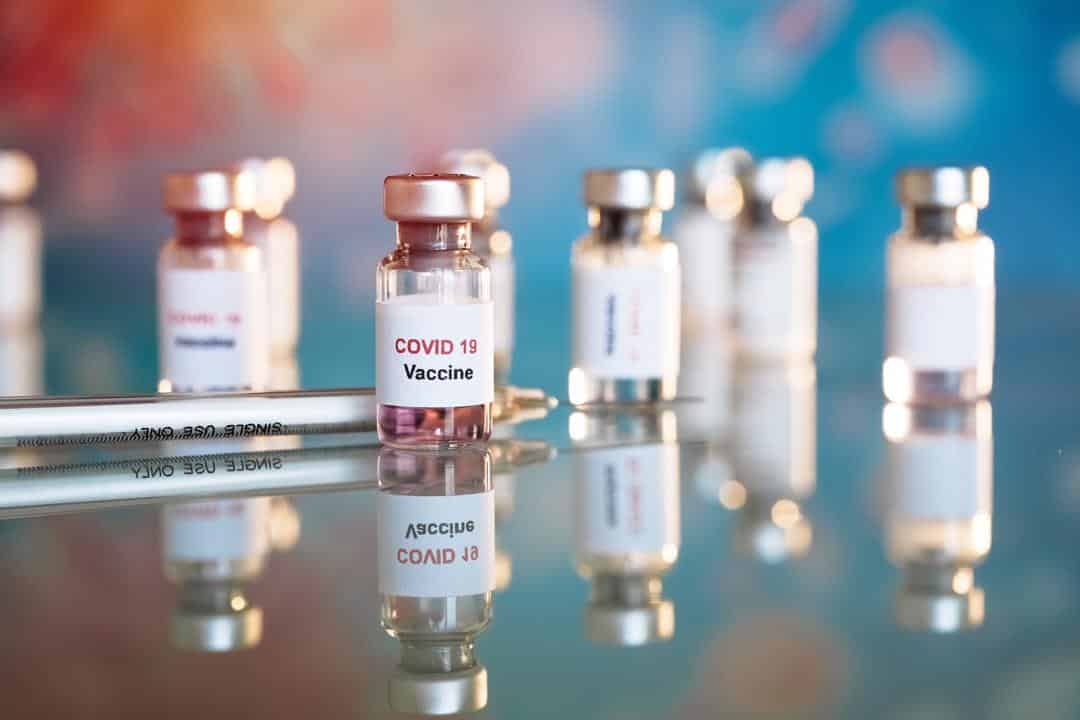
تم تعليق التجارب على لقاح لفيروس كورونا في الولايات المتحدة الأمريكية، بعد تعرض بعض المتطوعين خلال تجارب أجريت في بريطانيا لحالة صحية نادرة.
وأعرب الخبراء عن مخاوفهم بشأن تجارب اللقاح الذي تعمل عليه شركة AstraZeneca بعد أن أكدت الشركة أن اثنين من المتطوعين البريطانيين يعانون من أمراض عصبية خطيرة، وبسبب ذلك تم إيقاف الدراسة على اللقاح مرتين حتى الآن.
وقالت AstraZeneca: إن أول متطوع تلقى جرعة واحدة من اللقاح قبل أن يصاب بحالة نادرة من التهاب النخاع الشوكي، يعرف باسم التهاب النخاع المستعرض، وهو مرض التهابي نادر يتسبب في إصابة الحبل الشوكي بدرجات متفاوتة من الضعف والتغيرات الحسية والضعف اللاإرادي.
وأضافت الشركة أنها لم تتمكن من تأكيد نفس التشخيص لدى المريض الثاني، والذي تعرض لوعكة صحية بعد حصوله على الجرعة الثانية من اللقاح، لكن شخصًا مطلعًا أكد لصحيفة التايمز البريطانية تشخيص إصابة المريض الثاني بالتهاب النخاع المستعرض.
وقال مارك سليفكا، خبير اللقاحات في جامعة أوريغون للصحة والعلوم: “إذا كانت هناك حالتان حتى الآن، فسيبدأ هذا المرض في الظهور كنمط خطير، وإذا ظهرت حالة ثالثة من المرض العصبي بين المتطوعين، فسيتم إيقاف العمل على هذا اللقاح”.
وبعد توقف قصير، استؤنفت التجارب على اللقاح في بريطانيا والبرازيل والهند وجنوب إفريقيا، لكنها لا تزال متوقفة في الولايات المتحدة. وتلقى حوالي 18000 شخص في جميع أنحاء العالم لقاح AstraZeneca حتى الآن، بحسب ما ذكرت صحيفة نيويورك تايمز.
وينص المخطط التجريبي المكون من 111 صفحة للقاح على أن الهدف هو الحصول على لقاح فعال بنسبة 50%، وفي حال تحقيق هذا الهدف، فقد يكون من الممكن للشركة إيقاف التجارب مبكرًا، والتقدم بطلب للحصول على إذن من الحكومة لإطلاق اللقاح للاستخدام الطارئ.
وذكرت ورقة معلومات للمشاركين مؤرخة في 11 سبتمبر (أيلول) أن من غير المرجح أن تكون الأعراض التي ظهرت لدى بعض المتطوعين مرتبطة باللقاح، ولم يكن هناك دليل كافٍ للقول على وجه اليقين بأن المرض كان نتيجة اللقاح أو مرتبط به، وفي اليوم التالي أعلنت الشركة أنها استأنفت تجاربها في بريطانيا، في حين لم يسمح لها بمتابعة العمل في الولايات المتحدة، بحسب صحيفة ميرور البريطانية.